乙肝治疗的新曙光:mRNA和基因编辑能否带来治愈?
来源:
|
作者:li
|
发布时间: 112天前
|
168 次浏览
|
🔊 点击朗读正文
❚❚
▶
|
分享到:

慢性乙型肝炎病毒(HBV)感染影响着全球近3亿人,是导致肝硬化和肝癌的主要病因。尽管现有核苷(酸)类似物能有效抑制病毒复制,却难以实现“功能性治愈”——即在停止治疗后,乙肝表面抗原(HBsAg)持续检测不到,并伴随或不伴随乙肝表面抗体(抗-HBs)的出现。近期,一篇发表于《Advanced Drug Delivery Reviews》的深度综述,系统性地梳理了以mRNA疫苗和基因编辑为代表的下一代HBV治疗策略所取得的突破性进展,并坦诚剖析了通往临床应用所必须跨越的科学、监管与商业化鸿沟。本文将为您解读这一前沿领域的机遇与挑战。
一、 新一代疗法:从免疫激活到基因根除
该综述指出,当前研发管线中的核心策略主要分为两大方向:
免疫重建与激活:旨在打破慢性感染中宿主免疫系统的“耗竭”状态。
治疗性mRNA疫苗:作为明星技术,mRNA疫苗能够高效递送编码HBV抗原(如S、C、X蛋白)的指令至人体细胞,诱导强大的、多特异性的T细胞和B细胞反应。特别是自扩增型mRNA(saRNA)平台,因其能在细胞内自我复制,以更低剂量即可产生更强、更持久的免疫应答,被视为极具潜力的候选者。其目标不仅是控制病毒,更是清除被感染的肝细胞并建立长期免疫记忆。
其他免疫调节剂:包括检查点抑制剂(如PD-1/PD-L1抗体)、TLR激动剂等,旨在直接“唤醒”功能失调的HBV特异性T细胞。
直接靶向病毒基因组:旨在从源头上摧毁或沉默cccDNA(共价闭合环状DNA),这是HBV在肝细胞核内建立的持久性“病毒库”。
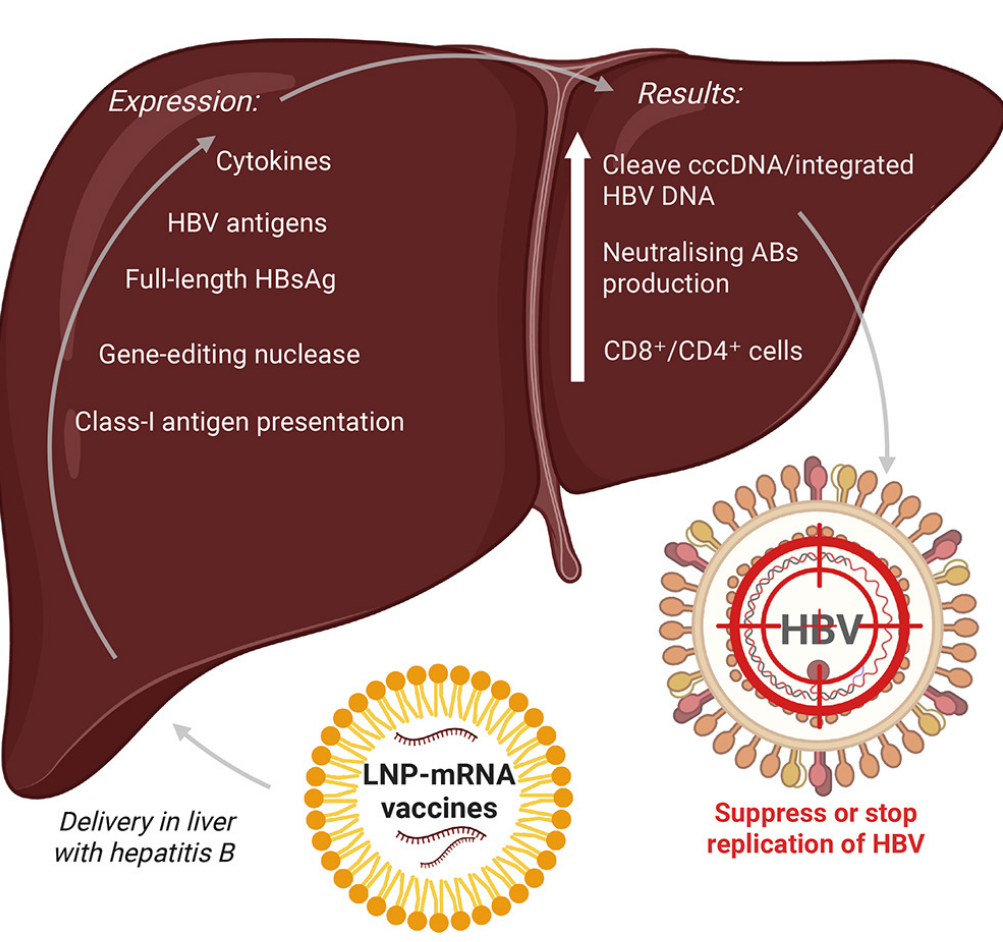
二、 前景光明,但荆棘密布
尽管上述策略在临床前和早期临床试验中展现出令人振奋的潜力,但综述作者也明确指出,要将这些尖端科技转化为安全有效的临床产品,仍面临严峻挑战。
安全性考量:
基因编辑的脱靶风险:像PBGENE-HBV这样的基因编辑疗法,其最大的担忧在于对非目标基因组位点的意外切割(脱靶效应),以及编辑后的DNA片段发生不可控的基因组整合,这可能诱发致癌突变。因此,需要极其严格的临床前安全谱型分析和长期的患者随访监测。
免疫疗法的免疫病理风险:强力激活的T细胞在清除受感染肝细胞的同时,也可能引发剧烈的肝脏炎症(肝炎发作),尤其是在高病毒载量或已有肝损伤的患者中。因此,精确的剂量控制和严格的患者筛选标准至关重要。
疗效障碍:
T细胞耗竭的深度:许多慢性HBV患者体内的HBV特异性T细胞已处于深度耗竭甚至被删除的状态,尤其在老年患者或高抗原负荷人群中,免疫疗法的响应率较低。克服这一障碍可能需要个体化的联合治疗方案,例如先用RNAi/ASO大幅降低抗原水平,再辅以mRNA疫苗进行免疫重建。
cccDNA的顽固性:cccDNA在肝细胞核内极其稳定,且其微染色体结构使其对许多药物具有天然抵抗力。如何高效、彻底地清除或永久沉默cccDNA,仍是所有直接抗病毒策略面临的终极难题。
监管与商业化挑战:
“功能性治愈”的定义与验证:监管机构(如FDA、EMA)要求证明HBsAg在停药后能长期维持阴性,这需要设计包含长时间随访期(通常1-2年甚至更长)的临床试验,大大增加了研发成本和时间。
新型疗法的监管框架尚在完善:mRNA疗法、基因编辑产品均为“同类首创”(first-in-class)的创新模式,全球监管机构仍在积极制定针对其生产工艺质量控制、临床试验设计、上市后药物警戒等方面的专门指南。这种监管环境的不确定性,使得从I期临床到最终获批的路径可能长达十年或更久。
三、 展望未来
综述最后强调,尽管道路漫长且充满挑战,但以mRNA疫苗、基因编辑、RNAi等为代表的新一代HBV疗法,正以前所未有的速度从实验室走向临床。未来几年将是决定这些突破性技术能否成功转化的关键窗口期。通过全球科研界、产业界与监管机构的紧密合作,我们有理由相信,为数亿慢性乙肝患者带来功能性治愈乃至完全治愈的希望,正在变得越来越清晰。
声明:本网所有转载文章内容为了宣传行业动态所用,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。